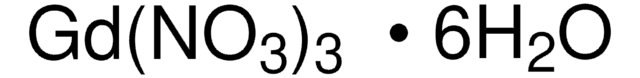238538
Cer(III)-nitrat Hexahydrat
99% trace metals basis
Synonym(e):
Certrinitrat, Salpetersäure-Cersalz
About This Item
Empfohlene Produkte
Qualitätsniveau
Assay
99% trace metals basis
Form
crystals and lumps
Eignung der Reaktion
reagent type: catalyst
core: cerium
Verunreinigungen
1-2% La
SMILES String
[Ce+3].[H]O[H].[H]O[H].[H]O[H].[H]O[H].[H]O[H].[H]O[H].[O-][N+]([O-])=O.[O-][N+]([O-])=O.[O-][N+]([O-])=O
InChI
1S/Ce.3NO3.6H2O/c;3*2-1(3)4;;;;;;/h;;;;6*1H2/q+3;3*-1;;;;;;
InChIKey
QQZMWMKOWKGPQY-UHFFFAOYSA-N
Suchen Sie nach ähnlichen Produkten? Aufrufen Leitfaden zum Produktvergleich
Allgemeine Beschreibung
Anwendung
Cerdioxid ist eine der am besten untersuchten Materialplattformen für die Katalyse und Festoxidbrennstoffzellen. Folglich entwickelten Wissenschaftler gut kontrollierte synthetische Protokolle mit Cer(III)-nitrat-hexahydrat zum Herstellen von Cerdioxid-Nanopartikeln, einschließlich Nano Cubes, Nanoröhrchen und Nanodrähte. Die anpassbare Synthese ermöglicht die Verwendung von Cerdioxid als Katalysatorträger, zum Beispiel zum Nutzen der Porosität der Mikrostruktur, um Metalle und Metalllegierungen zu imprägnieren, oder um beispielsweise Materialien auf Cerdioxid-Basis wie Cerdioxid-Zirkoniumdioxid zu synthetisieren.
Signalwort
Danger
H-Sätze
Gefahreneinstufungen
Aquatic Acute 1 - Aquatic Chronic 1 - Eye Dam. 1
Lagerklassenschlüssel
5.1B - Oxidizing hazardous materials
WGK
WGK 2
Flammpunkt (°F)
Not applicable
Flammpunkt (°C)
Not applicable
Persönliche Schutzausrüstung
Eyeshields, Gloves, type P3 (EN 143) respirator cartridges
Hier finden Sie alle aktuellen Versionen:
Analysenzertifikate (COA)
Die passende Version wird nicht angezeigt?
Wenn Sie eine bestimmte Version benötigen, können Sie anhand der Lot- oder Chargennummer nach einem spezifischen Zertifikat suchen.
Besitzen Sie dieses Produkt bereits?
In der Dokumentenbibliothek finden Sie die Dokumentation zu den Produkten, die Sie kürzlich erworben haben.
Kunden haben sich ebenfalls angesehen
Artikel
The rare earth elements impact nearly everyone in the world. All of the people living in advanced technological countries and almost all those living in third world countries utilize the rare earths in their everyday living—the car that one drives (gasoline is refined from oil using rare earth catalysts and catalytic converters reduce the polluting emissions from the automotive exhaust), watching the news on TV (the red and green colors in TV screens), the telephones and computers we use to communicate (the permanent magnets in speakers and disc drives), just to name a few examples.
Unser Team von Wissenschaftlern verfügt über Erfahrung in allen Forschungsbereichen einschließlich Life Science, Materialwissenschaften, chemischer Synthese, Chromatographie, Analytik und vielen mehr..
Setzen Sie sich mit dem technischen Dienst in Verbindung.