M3529
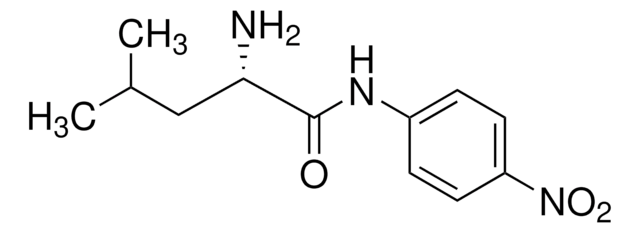
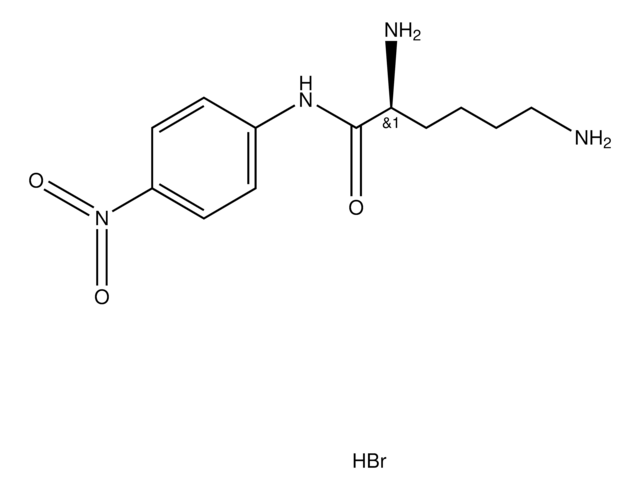
L-Methionine p-nitroanilide
≥98% (TLC), suitable for ligand binding assays
About This Item
Prodotti consigliati
Nome del prodotto
L-Methionine p-nitroanilide,
Saggio
≥98% (TLC)
Stato
powder
tecniche
ligand binding assay: suitable
Colore
white to faint yellow
Temperatura di conservazione
−20°C
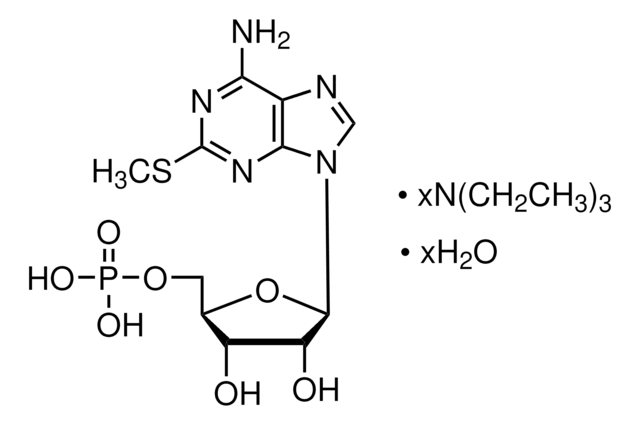
Stringa SMILE
CSCC[C@H](N)C(=O)Nc1ccc(cc1)[N+]([O-])=O
InChI
1S/C11H15N3O3S/c1-18-7-6-10(12)11(15)13-8-2-4-9(5-3-8)14(16)17/h2-5,10H,6-7,12H2,1H3,(H,13,15)/t10-/m0/s1
PLBWRAWSHVJPTL-JTQLQIEISA-N
Cerchi prodotti simili? Visita Guida al confronto tra prodotti
Categorie correlate
Azioni biochim/fisiol
Codice della classe di stoccaggio
11 - Combustible Solids
Classe di pericolosità dell'acqua (WGK)
WGK 3
Punto d’infiammabilità (°F)
Not applicable
Punto d’infiammabilità (°C)
Not applicable
Scegli una delle versioni più recenti:
Certificati d'analisi (COA)
Non trovi la versione di tuo interesse?
Se hai bisogno di una versione specifica, puoi cercare il certificato tramite il numero di lotto.
Possiedi già questo prodotto?
I documenti relativi ai prodotti acquistati recentemente sono disponibili nell’Archivio dei documenti.
Il team dei nostri ricercatori vanta grande esperienza in tutte le aree della ricerca quali Life Science, scienza dei materiali, sintesi chimica, cromatografia, discipline analitiche, ecc..
Contatta l'Assistenza Tecnica.