T0699
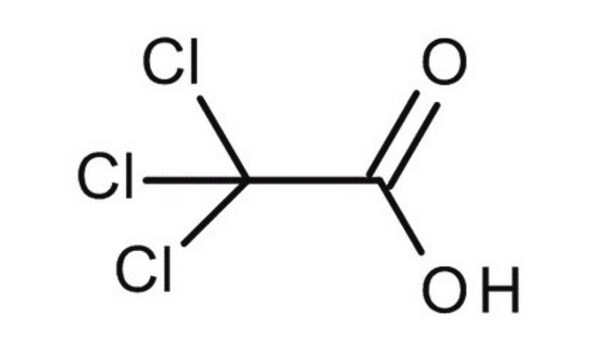
Acide trichloroacétique solution
6.1 N
Synonyme(s) :
TCA
About This Item
Produits recommandés
Forme
liquid
Niveau de qualité
Concentration
6.1 N
~100 % (w/v)
Chaîne SMILES
OC(=O)C(Cl)(Cl)Cl
InChI
1S/C2HCl3O2/c3-2(4,5)1(6)7/h(H,6,7)
Clé InChI
YNJBWRMUSHSURL-UHFFFAOYSA-N
Vous recherchez des produits similaires ? Visite Guide de comparaison des produits
Description générale
Application
- dans un essai avec l'enzyme indoleamine 2,3-dioxygénase (IDO) pour hydrolyser de la N-formylkynurénine et produire de la kynurénine.
- pour faire proliférer des cellules musculaires lisses d'artère pulmonaire humaine (HPASMC).
- pour traiter des tissus broyés et faire précipiter des protéines durant une extraction de protéines en vue de leur quantification.
Actions biochimiques/physiologiques
Mention d'avertissement
Danger
Mentions de danger
Conseils de prudence
Classification des risques
Aquatic Acute 1 - Aquatic Chronic 1 - Eye Dam. 1 - Skin Corr. 1A - STOT SE 3
Organes cibles
Respiratory system
Code de la classe de stockage
8A - Combustible corrosive hazardous materials
Classe de danger pour l'eau (WGK)
WGK 2
Point d'éclair (°F)
Not applicable
Point d'éclair (°C)
Not applicable
Faites votre choix parmi les versions les plus récentes :
Déjà en possession de ce produit ?
Retrouvez la documentation relative aux produits que vous avez récemment achetés dans la Bibliothèque de documents.
Articles
Proteinase K (EC 3.4.21.64) activity can be measured spectrophotometrically using hemoglobin as the substrate. Proteinase K hydrolyzes hemoglobin denatured with urea, and liberates Folin-postive amino acids and peptides. One unit will hydrolyze hemoglobin to produce color equivalent to 1.0 μmol of tyrosine per minute at pH 7.5 at 37 °C (color by Folin & Ciocalteu's Phenol Reagent).
Proteinase K (EC 3.4.21.64) activity can be measured spectrophotometrically using hemoglobin as the substrate. Proteinase K hydrolyzes hemoglobin denatured with urea, and liberates Folin-postive amino acids and peptides. One unit will hydrolyze hemoglobin to produce color equivalent to 1.0 μmol of tyrosine per minute at pH 7.5 at 37 °C (color by Folin & Ciocalteu's Phenol Reagent).
Protocoles
Objective: To standardize a procedure for the enzymatic determination of Glucose-6-phosphatase activity
This procedure may be used for determination of Pepsin activity using hemoglobin as the substrate. It is a spectrophotometric stop rate determination.
This procedure may be used for the determination of Amyloglucosidase activity using starch as the substrate.
To standardize a procedure for the determination of the enzymatic assay of choloylglycine hydrolase.
Notre équipe de scientifiques dispose d'une expérience dans tous les secteurs de la recherche, notamment en sciences de la vie, science des matériaux, synthèse chimique, chromatographie, analyse et dans de nombreux autres domaines..
Contacter notre Service technique