03449
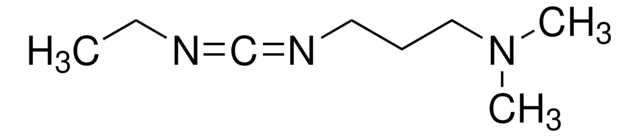
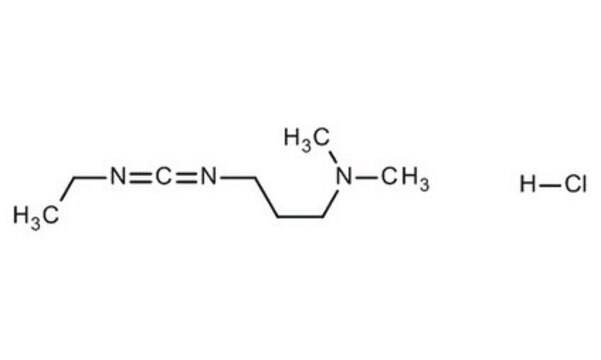
N-(3-Diméthylaminopropyl)-N′-éthylcarbodiimide hydrochloride
≥99.0% (AT)
Synonyme(s) :
N-Éthyl-N′-(3-diméthylaminopropyl) carbodiimide hydrochloride, EDAC, EDC, EDC hydrochloride, WSC hydrochloride
About This Item
Produits recommandés
Niveau de qualité
Pureté
≥99.0% (AT)
Forme
powder
Technique(s)
bioconjugation: suitable
Pf
110-115 °C (lit.)
112-116 °C
Solubilité
H2O: soluble 0.2 g/L
Température de stockage
−20°C
Chaîne SMILES
Cl.CCN=C=NCCCN(C)C
InChI
1S/C8H17N3.ClH/c1-4-9-8-10-6-5-7-11(2)3;/h4-7H2,1-3H3;1H
Clé InChI
FPQQSJJWHUJYPU-UHFFFAOYSA-N
Vous recherchez des produits similaires ? Visite Guide de comparaison des produits
Description générale
De plus, l'EDAC HCl permet de générer des ponts sur les biomolécules où il sert d'agent réticulant et relie les esters NHS à amine réactive des biomolécules aux groupements carboxyle. Cette technique s'avère intéressante pour la conjugaison des protéines, domaine dans lequel elle permet de créer des molécules hybrides avec de nouvelles propriétés et de nouvelles fonctions. Le mécanisme sous-jacent implique la réaction de l'EDAC HCl avec un groupement carboxyle, formant un intermédiaire instable qui cherche activement un partenaire aminé. L'équilibre délicat de cette réaction souligne l'importance d'optimiser les conditions pour assurer une conjugaison efficace. La présence de N-hydroxysuccinimide (NHS) renforce les capacités de l'EDAC HCl en stabilisant l'intermédiaire et en permettant de réaliser une conjugaison en deux étapes. Cela offre une plus grande flexibilité et un meilleur contrôle, en particulier avec les biomolécules complexes.
Application
Actions biochimiques/physiologiques
Caractéristiques et avantages
Autres remarques
Produit comparable
Mention d'avertissement
Danger
Mentions de danger
Conseils de prudence
Classification des risques
Acute Tox. 3 Dermal - Acute Tox. 4 Oral - Aquatic Acute 1 - Aquatic Chronic 1 - Skin Irrit. 2 - Skin Sens. 1 - STOT RE 2 Oral
Organes cibles
Stomach,large intestine,lymph node
Code de la classe de stockage
6.1C - Combustible acute toxic Cat.3 / toxic compounds or compounds which causing chronic effects
Classe de danger pour l'eau (WGK)
WGK 3
Point d'éclair (°F)
Not applicable
Point d'éclair (°C)
Not applicable
Équipement de protection individuelle
dust mask type N95 (US), Eyeshields, Gloves
Certificats d'analyse (COA)
Recherchez un Certificats d'analyse (COA) en saisissant le numéro de lot du produit. Les numéros de lot figurent sur l'étiquette du produit après les mots "Lot" ou "Batch".
Déjà en possession de ce produit ?
Retrouvez la documentation relative aux produits que vous avez récemment achetés dans la Bibliothèque de documents.
Les clients ont également consulté
Articles
Carbodiimide-mediated peptide coupling remains to the most frequently used technique.
The detection and quantification of biomarkers are essential for medical diagnostics, environmental monitoring, and bioresearch.
Amide bonds are ubiquitous in both nature and industrial applications. They are vital to the structure and function of biological macromolecules and polymers. The importance of this functionality has resulted in numerous approaches to its formation, ranging from stoichiometric activation of carboxylic acids to more recent advances in catalytic amide bond formation.
Professor Aran (Claremont University, USA) thoroughly discusses the engineering of graphene based materials through careful functionalization of graphene oxide, a solution processable form of graphene.
Notre équipe de scientifiques dispose d'une expérience dans tous les secteurs de la recherche, notamment en sciences de la vie, science des matériaux, synthèse chimique, chromatographie, analyse et dans de nombreux autres domaines..
Contacter notre Service technique






![1-[3-(Dimethylamino)propyl]-3-ethylcarbodiimide methiodide](/deepweb/assets/sigmaaldrich/product/structures/414/134/4eb9c126-d7f9-4e12-9e3a-95cb077824fd/640/4eb9c126-d7f9-4e12-9e3a-95cb077824fd.png)