670871
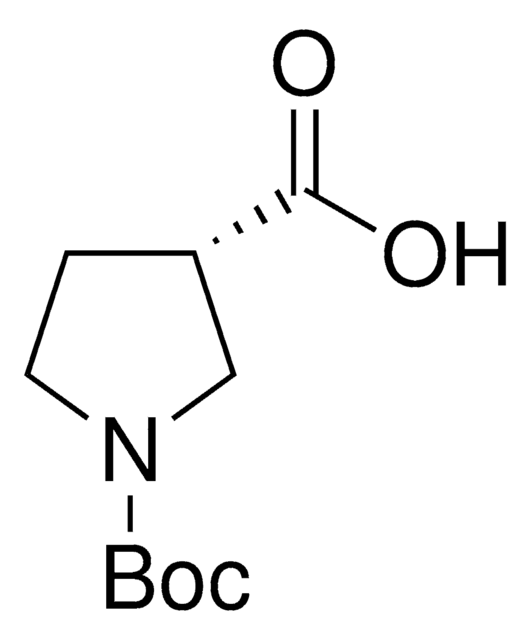
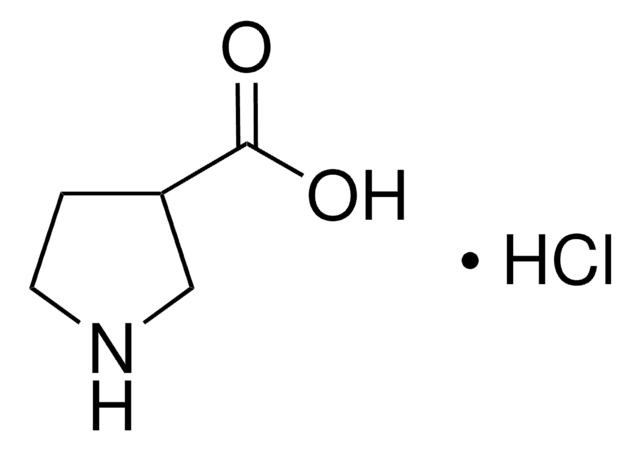
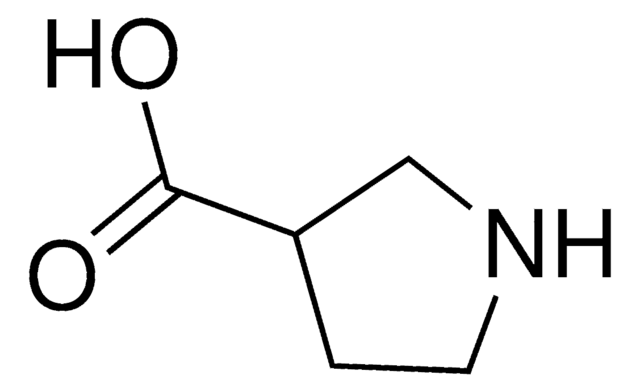
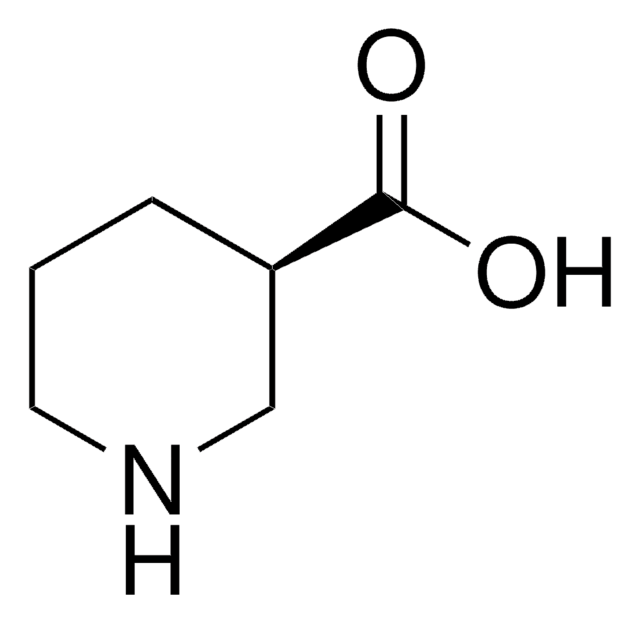
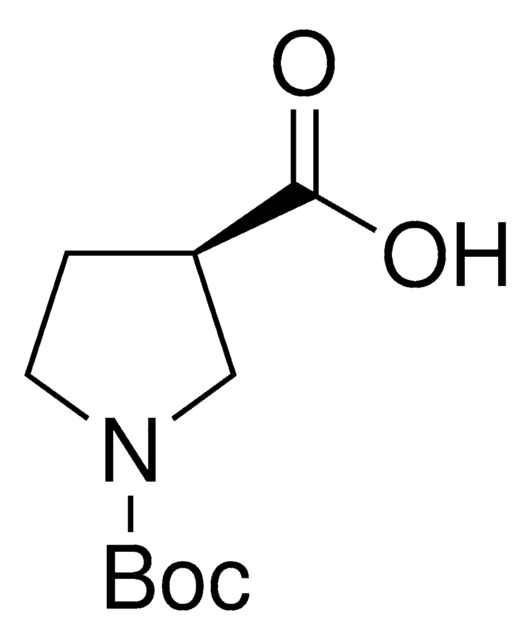
(S)-(+)-Pyrrolidine-3-carboxylic acid
≥98.0% (NT)
Synonyme(s) :
(S)-β-Proline
About This Item
Produits recommandés
Pureté
≥98.0% (NT)
Forme
solid
Activité optique
[α]/D 20.0±2.0°, c = 2 in H2O
Capacité de réaction
reaction type: solution phase peptide synthesis
Application(s)
peptide synthesis
Température de stockage
2-8°C
Chaîne SMILES
OC(=O)[C@H]1CCNC1
InChI
1S/C5H9NO2/c7-5(8)4-1-2-6-3-4/h4,6H,1-3H2,(H,7,8)/t4-/m0/s1
Clé InChI
JAEIBKXSIXOLOL-BYPYZUCNSA-N
Catégories apparentées
Code de la classe de stockage
11 - Combustible Solids
Classe de danger pour l'eau (WGK)
WGK 3
Point d'éclair (°F)
Not applicable
Point d'éclair (°C)
Not applicable
Équipement de protection individuelle
Eyeshields, Gloves, type N95 (US)
Faites votre choix parmi les versions les plus récentes :
Certificats d'analyse (COA)
Vous ne trouvez pas la bonne version ?
Si vous avez besoin d'une version particulière, vous pouvez rechercher un certificat spécifique par le numéro de lot.
Déjà en possession de ce produit ?
Retrouvez la documentation relative aux produits que vous avez récemment achetés dans la Bibliothèque de documents.
Les clients ont également consulté
Notre équipe de scientifiques dispose d'une expérience dans tous les secteurs de la recherche, notamment en sciences de la vie, science des matériaux, synthèse chimique, chromatographie, analyse et dans de nombreux autres domaines..
Contacter notre Service technique