D1411
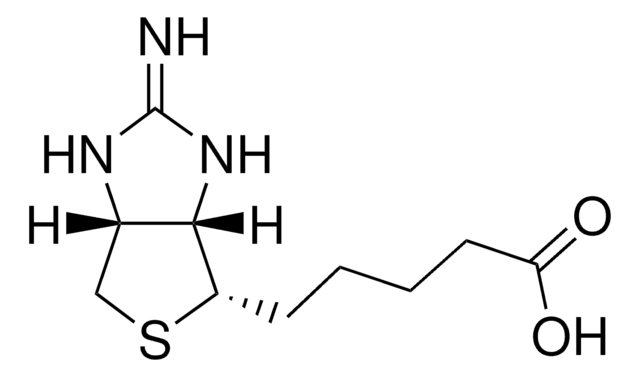
D-Destiobiotina
≥98% (TLC)
Sinónimos:
Ácido 5-metil-2-oxo-4-imidazolidinohexanoico
Iniciar sesiónpara Ver la Fijación de precios por contrato y de la organización
About This Item
Fórmula empírica (notación de Hill):
C10H18N2O3
Número de CAS:
Peso molecular:
214.26
Número CE:
Número MDL:
Código UNSPSC:
12352200
eCl@ss:
34058011
ID de la sustancia en PubChem:
NACRES:
NA.25
Productos recomendados
Ensayo
≥98% (TLC)
Formulario
powder
temp. de almacenamiento
2-8°C
cadena SMILES
C[C@@H]1NC(=O)N[C@@H]1CCCCCC(O)=O
InChI
1S/C10H18N2O3/c1-7-8(12-10(15)11-7)5-3-2-4-6-9(13)14/h7-8H,2-6H2,1H3,(H,13,14)(H2,11,12,15)/t7-,8+/m0/s1
Clave InChI
AUTOLBMXDDTRRT-JGVFFNPUSA-N
Aplicación
La d-destiobiotina se ha utilizado como componente de los tampones de elución:
- para eluir las proteínas precipitadas de la resina durante la coinmunoprecipitación
- para eluir la helicasa Cdc45-MCM-GINS (CMG) humana durante la purificación cromatográfica de las proteínas
- para eluir el miembro 3A/B de la familia de cinesinas heterodímeras (KIF3A/B) y el dominio armadillo APC de unión a la proteína asociada a la cinesina 3 (KAP3) durante la purificación cromatográfica
La d-destiobiotina se utiliza en la cromatografía de afinidad y la cromatografía de proteínas. La d-destiobiotina puede utilizarse para marcaje, detección y aislamiento de proteínas.
Acciones bioquímicas o fisiológicas
La destiobiotina es un derivado de la biotina que no contiene azufre, que se une con menos fuerza a las proteínas de unión a la biotina y que es disociada fácilmente por la biotina.
Código de clase de almacenamiento
11 - Combustible Solids
Clase de riesgo para el agua (WGK)
WGK 3
Punto de inflamabilidad (°F)
Not applicable
Punto de inflamabilidad (°C)
Not applicable
Equipo de protección personal
Eyeshields, Gloves, type N95 (US)
Elija entre una de las versiones más recientes:
¿Ya tiene este producto?
Encuentre la documentación para los productos que ha comprado recientemente en la Biblioteca de documentos.
Teegan A Delli-Bovi et al.
BMC biotechnology, 10, 73-73 (2010-10-13)
Biotin is an essential enzyme cofactor that acts as a CO2 carrier in carboxylation and decarboxylation reactions. The E. coli genome encodes a biosynthetic pathway that produces biotin from pimeloyl-CoA in four enzymatic steps. The final step, insertion of sulfur
Bi-Huang Hu et al.
Analytical chemistry, 79(19), 7275-7285 (2007-08-24)
We describe a new method for encoded synthesis, efficient on-resin screening, and rapid unambiguous sequencing of combinatorial peptide libraries. An improved binary tag system for encoding peptide libraries during synthesis was designed to facilitate unequivocal assignment of isobaric residues by
Rocio Rodriguez-Melendez et al.
The Journal of nutrition, 133(5), 1259-1264 (2003-05-06)
In mammals, biotin serves as a coenzyme for carboxylases such as propionyl-CoA carboxylase. The expression of genes encoding interleukin-2 (IL-2) and IL-2 receptor (IL-2R)gamma also depends on biotin. Biotin metabolites are structurally similar to biotin, and their concentrations in tissues
M Sárdy et al.
Clinical chemistry, 45(12), 2142-2149 (1999-12-10)
Tissue transglutaminase (TGc) has recently been identified as the major, if not the sole, autoantigen of gluten-sensitive enteropathy (GSE). We developed and validated an ELISA based on the human recombinant antigen and compared it to existing serological tests for GSE
Sudha Purushothaman et al.
PloS one, 3(5), e2320-e2320 (2008-05-30)
Fatty acids are indispensable constituents of mycolic acids that impart toughness & permeability barrier to the cell envelope of M. tuberculosis. Biotin is an essential co-factor for acetyl-CoA carboxylase (ACC) the enzyme involved in the synthesis of malonyl-CoA, a committed
Nuestro equipo de científicos tiene experiencia en todas las áreas de investigación: Ciencias de la vida, Ciencia de los materiales, Síntesis química, Cromatografía, Analítica y muchas otras.
Póngase en contacto con el Servicio técnico