A6888
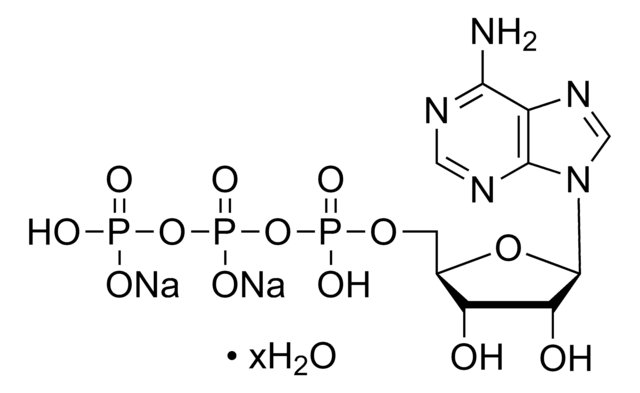
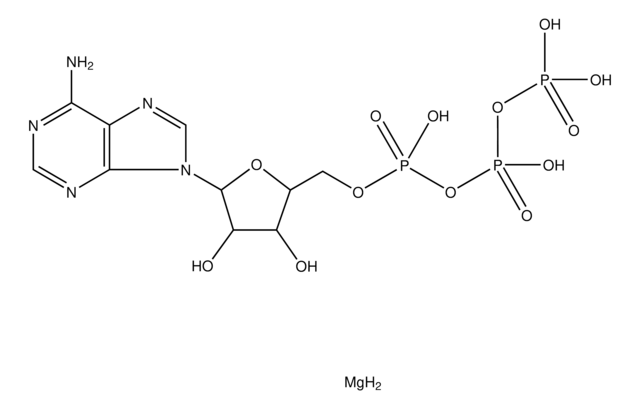
Adenosine 5′-triphosphate–Agarose
aqueous glycerol suspension
Iniciar sesiónpara Ver la Fijación de precios por contrato y de la organización
About This Item
Productos recomendados
Formulario
aqueous glycerol suspension
Nivel de calidad
Extensión del etiquetado
≥1 μmol per mL
Matriz
cross-linked 4% beaded agarose
activación de la matriz
cyanogen bromide
unión a la matriz
ribose hydroxyls
espaciador de matriz
11 atoms (adipic acid dihydrazide)
temp. de almacenamiento
−20°C
¿Está buscando productos similares? Visita Guía de comparación de productos
Aplicación
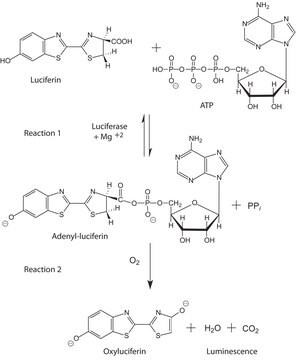
Adenosine 5′-triphosphate Agarose (5′-ATP agarose) has been used in affinity chromatography to purify uridine kinase from Ehrlich ascites tumor cells.
Forma física
Suspension in 50% glycerol containing 0.25 M NaCl
Código de clase de almacenamiento
10 - Combustible liquids
Clase de riesgo para el agua (WGK)
WGK 3
Punto de inflamabilidad (°F)
Not applicable
Punto de inflamabilidad (°C)
Not applicable
Elija entre una de las versiones más recientes:
Certificados de análisis (COA)
Lot/Batch Number
¿No ve la versión correcta?
Si necesita una versión concreta, puede buscar un certificado específico por el número de lote.
¿Ya tiene este producto?
Encuentre la documentación para los productos que ha comprado recientemente en la Biblioteca de documentos.
B L Stitt
The Journal of biological chemistry, 263(23), 11130-11137 (1988-08-15)
We have determined that 3 mol of ATP or other adenine nucleotide can bind to Escherichia coli transcription termination protein rho, in the presence or absence of the RNA cofactor that is required for activation of rho's ATPase activity. Isotope
S Ogg et al.
The Journal of biological chemistry, 269(48), 30461-30469 (1994-12-02)
Human Cdc25C is a protein phosphatase that dephosphorylates and activates Cdc2-cyclin B to trigger entry into mitosis. Cdc25C is itself regulated by phosphorylation. In asynchronously growing HeLa cells, we have determined that serine 216 is the major site of Cdc25C
V Nagaraja et al.
Journal of molecular biology, 182(4), 579-587 (1985-04-20)
We have purified the type I restriction enzymes SB and SP from Salmonella typhimurium and S. potsdam, respectively, and determined the DNA sequences that they recognize. These sequences resemble those previously determined for the type I enzymes, EcoB, EcoK and
H D Kim et al.
Biochemistry, 38(44), 14697-14710 (1999-11-05)
Two polynucleotide-dependent ATPases, 95 and 181 kDa in size, have been purified to near homogeneity from cell-free extracts of Schizosaccharomyces pombe. Despite their size differences, their biochemical properties were strikingly similar. Both enzymes were capable of unwinding RNA and DNA
B Suri et al.
The EMBO journal, 3(3), 575-579 (1984-03-01)
The EcoA restriction enzyme from Escherichia coli 15T- has been isolated. It proves to be an unusual enzyme, clearly related functionally to the classical type I restriction enzymes. The basic enzyme is a two subunit modification methylase. Another protein species
Nuestro equipo de científicos tiene experiencia en todas las áreas de investigación: Ciencias de la vida, Ciencia de los materiales, Síntesis química, Cromatografía, Analítica y muchas otras.
Póngase en contacto con el Servicio técnico