Wichtige Dokumente
D9779
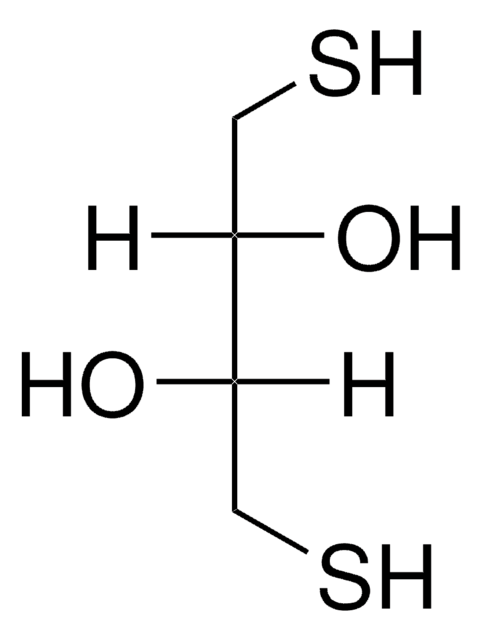
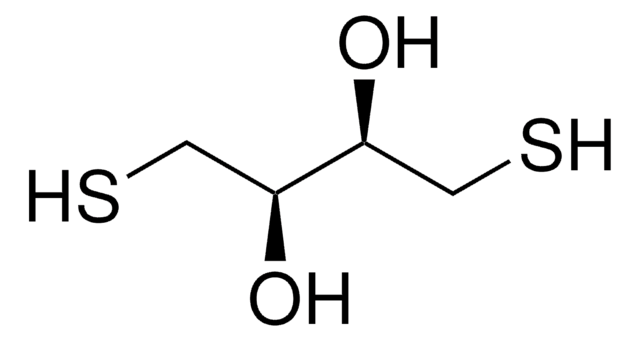
DL-Dithiothreitol
for molecular biology, ≥98% (HPLC), ≥99% (titration)
Synonym(e):
(±)-Dithiothreitol, rac-Dithiothreitol, Dithiothreitol, threo-1,4-Dimercapto-2,3-butandiol, Clelands Reagens, DTT
About This Item
Empfohlene Produkte
Qualität
Molecular Biology
for molecular biology
Assay
≥98% (HPLC)
≥99% (titration)
Form
powder
Eignung der Reaktion
reagent type: reductant
mp (Schmelzpunkt)
41-44 °C (lit.)
Löslichkeit
H2O: 50 mg/mL
Kationenspuren
heavy metals (as Pb): ≤5 ppm
Eignung
suitable for molecular biology
Fremdaktivität
DNase, RNase, protease, none detected
Lagertemp.
2-8°C
SMILES String
O[C@H](CS)[C@H](O)CS
InChI
1S/C4H10O2S2/c5-3(1-7)4(6)2-8/h3-8H,1-2H2/t3-,4-/m1/s1
InChIKey
VHJLVAABSRFDPM-QWWZWVQMSA-N
Suchen Sie nach ähnlichen Produkten? Aufrufen Leitfaden zum Produktvergleich
Allgemeine Beschreibung
Anwendung
Es wird wie folgt verwendet:
- als Komponente für die Proteinextraktion bei der Western-Blot-Analyse
- zur Vorbereitung von Proben-Lysepuffer für die quantitative Massenspektroskopie
- als Kinase-Pufferkomponente für das Enzymimmunoassay (ELISA)
Biochem./physiol. Wirkung
Leistungsmerkmale und Vorteile
- Geeignet für die Molekularbiologie
- Frei von RNase, DNase, Exonuklease und Protease
- Hohe Reinheit (HPLC ≥98 %)
- Kein Schwermetall ≤5 ppm
Sonstige Hinweise
Vergleichbares Produkt
Signalwort
Danger
H-Sätze
Gefahreneinstufungen
Acute Tox. 4 Oral - Eye Dam. 1 - Skin Irrit. 2
Lagerklassenschlüssel
11 - Combustible Solids
WGK
WGK 3
Flammpunkt (°F)
Not applicable
Flammpunkt (°C)
Not applicable
Persönliche Schutzausrüstung
dust mask type N95 (US), Eyeshields, Faceshields, Gloves
Hier finden Sie alle aktuellen Versionen:
Besitzen Sie dieses Produkt bereits?
In der Dokumentenbibliothek finden Sie die Dokumentation zu den Produkten, die Sie kürzlich erworben haben.
Kunden haben sich ebenfalls angesehen
Protokolle
Follow this DDT reduction protocol to reduce disulfide bonds in thiol-modified oligonucleotides, thereby avoiding this source of oligo dimer formation.
Unser Team von Wissenschaftlern verfügt über Erfahrung in allen Forschungsbereichen einschließlich Life Science, Materialwissenschaften, chemischer Synthese, Chromatographie, Analytik und vielen mehr..
Setzen Sie sich mit dem technischen Dienst in Verbindung.