Alle Fotos(3)
Wichtige Dokumente
D1411
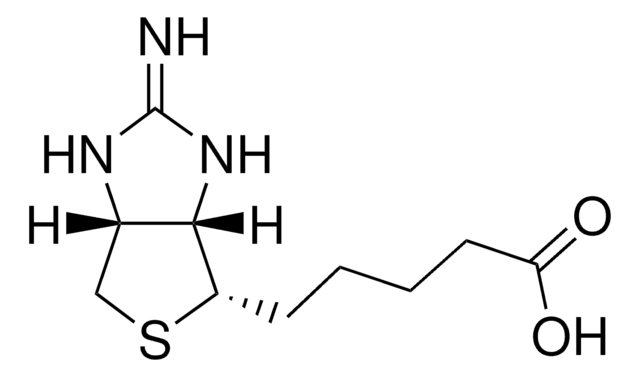
d-Desthiobiotin
≥98% (TLC)
Synonym(e):
5-Methyl-2-oxo-4-imidazolidinhexansäure
Anmeldenzur Ansicht organisationsspezifischer und vertraglich vereinbarter Preise
Alle Fotos(3)
About This Item
Empirische Formel (Hill-System):
C10H18N2O3
CAS-Nummer:
Molekulargewicht:
214.26
EG-Nummer:
MDL-Nummer:
UNSPSC-Code:
12352200
eCl@ss:
34058011
PubChem Substanz-ID:
NACRES:
NA.25
Empfohlene Produkte
Assay
≥98% (TLC)
Form
powder
Lagertemp.
2-8°C
SMILES String
C[C@@H]1NC(=O)N[C@@H]1CCCCCC(O)=O
InChI
1S/C10H18N2O3/c1-7-8(12-10(15)11-7)5-3-2-4-6-9(13)14/h7-8H,2-6H2,1H3,(H,13,14)(H2,11,12,15)/t7-,8+/m0/s1
InChIKey
AUTOLBMXDDTRRT-JGVFFNPUSA-N
Anwendung
d-Desthiobiotin wird als Komponente von Elutionspuffern für Folgendes eingesetzt:
- zum Eluieren der ausgefällten Proteine aus dem Harz während der Co-Immunpräzipitation
- zum Eluieren von humaner Cdc45-MCM-GINS(CMG)-Helikase während der chromatografischen Proteinaufreinigung
- zum Eluieren des heterodimeren Kinesin-Familienmitglieds 3A/B (KIF3A/B) und der Kinesin-assoziiertes-Protein-3(KAP3)-Bindungs-APC-Armadillo(APCARM)-Domäne während der chromatografischen Aufreinigung
d-Desthiobiotin wird in der Affinitätschromatografie und Proteinchromatografie verwendet. Es kann für Proteinmarkierung, -nachweis und -isolierung eingesetzt werden.
Biochem./physiol. Wirkung
Desthiobiotin ist ein nichtschwefelhaltiges Biotin-Derivat, das weniger stark an Biotin-Bindungsproteine bindet und leicht durch Biotin verdrängt wird.
Lagerklassenschlüssel
11 - Combustible Solids
WGK
WGK 3
Flammpunkt (°F)
Not applicable
Flammpunkt (°C)
Not applicable
Persönliche Schutzausrüstung
Eyeshields, Gloves, type N95 (US)
Hier finden Sie alle aktuellen Versionen:
Besitzen Sie dieses Produkt bereits?
In der Dokumentenbibliothek finden Sie die Dokumentation zu den Produkten, die Sie kürzlich erworben haben.
Teegan A Delli-Bovi et al.
BMC biotechnology, 10, 73-73 (2010-10-13)
Biotin is an essential enzyme cofactor that acts as a CO2 carrier in carboxylation and decarboxylation reactions. The E. coli genome encodes a biosynthetic pathway that produces biotin from pimeloyl-CoA in four enzymatic steps. The final step, insertion of sulfur
Bi-Huang Hu et al.
Analytical chemistry, 79(19), 7275-7285 (2007-08-24)
We describe a new method for encoded synthesis, efficient on-resin screening, and rapid unambiguous sequencing of combinatorial peptide libraries. An improved binary tag system for encoding peptide libraries during synthesis was designed to facilitate unequivocal assignment of isobaric residues by
Rocio Rodriguez-Melendez et al.
The Journal of nutrition, 133(5), 1259-1264 (2003-05-06)
In mammals, biotin serves as a coenzyme for carboxylases such as propionyl-CoA carboxylase. The expression of genes encoding interleukin-2 (IL-2) and IL-2 receptor (IL-2R)gamma also depends on biotin. Biotin metabolites are structurally similar to biotin, and their concentrations in tissues
M Sárdy et al.
Clinical chemistry, 45(12), 2142-2149 (1999-12-10)
Tissue transglutaminase (TGc) has recently been identified as the major, if not the sole, autoantigen of gluten-sensitive enteropathy (GSE). We developed and validated an ELISA based on the human recombinant antigen and compared it to existing serological tests for GSE
Sudha Purushothaman et al.
PloS one, 3(5), e2320-e2320 (2008-05-30)
Fatty acids are indispensable constituents of mycolic acids that impart toughness & permeability barrier to the cell envelope of M. tuberculosis. Biotin is an essential co-factor for acetyl-CoA carboxylase (ACC) the enzyme involved in the synthesis of malonyl-CoA, a committed
Unser Team von Wissenschaftlern verfügt über Erfahrung in allen Forschungsbereichen einschließlich Life Science, Materialwissenschaften, chemischer Synthese, Chromatographie, Analytik und vielen mehr..
Setzen Sie sich mit dem technischen Dienst in Verbindung.