T7409
Trypsine from porcine pancreas
lyophilized powder, Type II-S, 1,000-2,000 units/mg dry solid
Se connecterpour consulter vos tarifs contractuels et ceux de votre entreprise/organisme
About This Item
Produits recommandés
Type
Type II-S
Niveau de qualité
Forme
lyophilized powder
Activité spécifique
1,000-2,000 units/mg dry solid
Poids mol.
23.8 kDa
Température de stockage
−20°C
Vous recherchez des produits similaires ? Visite Guide de comparaison des produits
Catégories apparentées
Application
Pour la digestion trypsique des peptides, utiliser un rapport trypsine:peptide d'environ 1:100 à 1:20. La trypsine sert généralement à détacher les cellules adhérentes d'une surface de culture. La concentration qui permet de déloger les cellules de leur substrat dépend principalement du type de cellules et de l'âge de la culture. La trypsine a également été utilisée pour remettre des cellules en suspension lors de cultures cellulaires, pour digérer des protéines en recherche protéomique ou pour réaliser diverses digestions sur gel†. Parmi ses autres applications, citons l'analyse de la cristallisation par des techniques à membrane ou une étude visant à établir que le taux de repliement et le rendement des protéines peuvent être limités par la présence de pièges cinétiques.
Actions biochimiques/physiologiques
La trypsine clive les peptides situés du côté C-terminal des résidus lysine et arginine. Cette réaction d'hydrolyse est plus lente lorsqu'un résidu acide se situe d'un côté ou de l'autre du site de clivage, et elle s'interrompt lorsqu'un résidu proline se situe du côté carboxyle du site de clivage. L'activité de la trypsine est optimale à un pH de 7 à 9. La trypsine peut également cliver les liaisons ester et amide de dérivés d'acides aminés de synthèse. On ajoute de l'EDTA aux solutions de trypsine pour servir d'agent chélateur afin de neutraliser les ions calcium et magnésium qui masquent les liaisons peptidiques sur lesquelles la trypsine agit. L'élimination de ces ions augmente l'activité enzymatique.
Les inhibiteurs de protéases à sérine (entre autres, le DFP, la TLCK, l'APMSF, l'AEBSEF et l'aprotinine) inhibent la trypsine.
Les inhibiteurs de protéases à sérine (entre autres, le DFP, la TLCK, l'APMSF, l'AEBSEF et l'aprotinine) inhibent la trypsine.
Composants
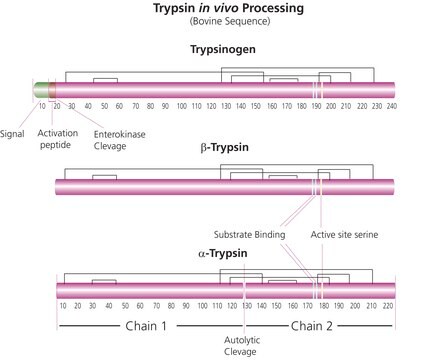
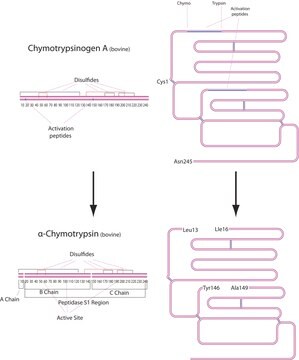
Trypsin consists of a single chain polypeptide of 223 amino acid residues, produced by the removal of the N-terminal hexapeptide from trypsinogen which is cleaved at the Lys - lle peptide bond. The sequence of amino acids is cross-linked by 6 disulfide bridges. This is the native form of trypsin, beta-trypsin. BETA-trypsin can be autolyzed, cleaving at the Lys - Ser residue, to produce alpha-trypsin. Trypsin is a member of the serine protease family.
Attention
Solutions in 1 mM HCl are stable for 1 year in aliquots and stored at -20°C. The presence of Ca2+ will also diminish the self-autolysis of trypsin and maintain its stability in solution. Trypsin will also retain most of its activity in 2.0 M urea, 2.0 M guanidine HCl, or 0.1% (w/v) SDS.
Définition de l'unité
Une unité de BAEE produit une ΔA253 de 0,001 par minute à pH 7,6 et à 25 °C lorsque le BAEE est utilisé comme substrat. 1 unité de BTEE = 320 unités d'ATEE. Volume réactionnel = 3,2 ml (trajet optique de 1 cm).
Notes préparatoires
This product is a lyophilized powder soluble in Hank′s Balanced Salt Solution at 25 mg/mL.
Inhibiteur
Réf. du produit
Description
Tarif
Substrat
Mention d'avertissement
Danger
Mentions de danger
Conseils de prudence
Classification des risques
Eye Irrit. 2 - Resp. Sens. 1 - Skin Irrit. 2 - STOT SE 3
Organes cibles
Respiratory system
Code de la classe de stockage
11 - Combustible Solids
Classe de danger pour l'eau (WGK)
WGK 1
Équipement de protection individuelle
dust mask type N95 (US), Eyeshields, Faceshields, Gloves
Faites votre choix parmi les versions les plus récentes :
Déjà en possession de ce produit ?
Retrouvez la documentation relative aux produits que vous avez récemment achetés dans la Bibliothèque de documents.
Les clients ont également consulté
Tanja Laske et al.
PLoS computational biology, 15(4), e1006944-e1006944 (2019-04-12)
The best measure to limit spread of contagious diseases caused by influenza A viruses (IAVs) is annual vaccination. The growing global demand for low-cost vaccines requires the establishment of high-yield production processes. One possible option to address this challenge is
Daniel Rüdiger et al.
PLoS computational biology, 15(2), e1006819-e1006819 (2019-02-20)
Influenza A viruses (IAV) are commonly used to infect animal cell cultures for research purposes and vaccine production. Their replication is influenced strongly by the multiplicity of infection (MOI), which ranges over several orders of magnitude depending on the respective
Fan Zhao et al.
Molecular nutrition & food research, 63(23), e1900589-e1900589 (2019-10-08)
The gut microbiota plays an essential role in linking diet to host health. The specific role of different dietary proteins on the gut microbiota and health is less understood. Here, the impact of proteins derived from chicken and soy on
Xiaoyu Zou et al.
Frontiers in nutrition, 7, 151-151 (2020-10-20)
In this work, we investigated changes in protein structures in vacuum-packed pork during chill storage and its impact on the in vitro protein digestion. Longissimus dorsi muscles were vacuum packed and stored at 4°C for 3 days. Samples were subjected
Shulin Zhang et al.
Autophagy, 13(8), 1318-1330 (2017-06-09)
Magnaporthe oryzae, the ascomycete fungus that causes rice blast disease, initiates conidiation in response to light when grown on Prune-Agar medium containing both carbon and nitrogen sources. Macroautophagy/autophagy was shown to be essential for M. oryzae conidiation and induced specifically
Notre équipe de scientifiques dispose d'une expérience dans tous les secteurs de la recherche, notamment en sciences de la vie, science des matériaux, synthèse chimique, chromatographie, analyse et dans de nombreux autres domaines..
Contacter notre Service technique