D1411
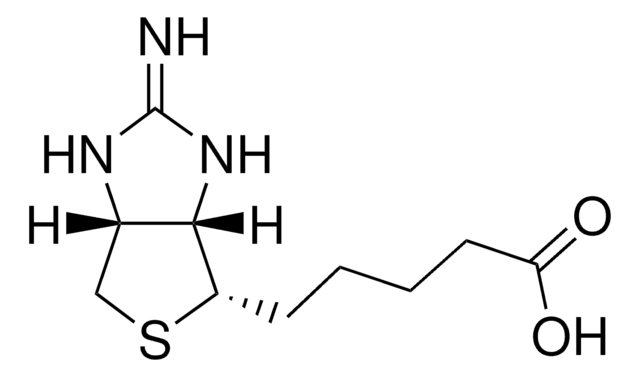
d-Déthiobiotine
≥98% (TLC)
Synonyme(s) :
Acide 5-méthyl-2-oxo-4-imidazolidine hexanoïque
Se connecterpour consulter vos tarifs contractuels et ceux de votre entreprise/organisme
About This Item
Formule empirique (notation de Hill) :
C10H18N2O3
Numéro CAS:
Poids moléculaire :
214.26
Numéro CE :
Numéro MDL:
Code UNSPSC :
12352200
eCl@ss :
34058011
ID de substance PubChem :
Nomenclature NACRES :
NA.25
Produits recommandés
Essai
≥98% (TLC)
Forme
powder
Température de stockage
2-8°C
Chaîne SMILES
C[C@@H]1NC(=O)N[C@@H]1CCCCCC(O)=O
InChI
1S/C10H18N2O3/c1-7-8(12-10(15)11-7)5-3-2-4-6-9(13)14/h7-8H,2-6H2,1H3,(H,13,14)(H2,11,12,15)/t7-,8+/m0/s1
Clé InChI
AUTOLBMXDDTRRT-JGVFFNPUSA-N
Application
La d-desthiobiotine a été ajoutée à des tampons d'élution :
- pour éluer des protéines précipitées à partir d'une résine durant une co-immunoprécipitation.
- pour éluer l'hélicase Cdc45–MCM–GINS (CMG) humaine lors de la purification de protéines par chromatographie.
- pour éluer le domaine APCARM (APC armadillo) de liaison à KIF3A/B (membre 3A/B hétérodimère de la famille des kinésines) et à KAP3 (protéine 3 associée aux kinésines) durant une purification chromatographique.
La d-déthiobiotine est utilisée dans la chromatographie d'affinité et la chromatographie de protéines. Elle peut être utilisée pour marquer, détecter et isoler des protéines.
Actions biochimiques/physiologiques
La desthiobiotine est un dérivé de biotine exempt de soufre qui se fixe moins fortement aux protéines se liant à la biotine et qui est facilement délogé par cette dernière.
Code de la classe de stockage
11 - Combustible Solids
Classe de danger pour l'eau (WGK)
WGK 3
Point d'éclair (°F)
Not applicable
Point d'éclair (°C)
Not applicable
Équipement de protection individuelle
Eyeshields, Gloves, type N95 (US)
Faites votre choix parmi les versions les plus récentes :
Déjà en possession de ce produit ?
Retrouvez la documentation relative aux produits que vous avez récemment achetés dans la Bibliothèque de documents.
Teegan A Delli-Bovi et al.
BMC biotechnology, 10, 73-73 (2010-10-13)
Biotin is an essential enzyme cofactor that acts as a CO2 carrier in carboxylation and decarboxylation reactions. The E. coli genome encodes a biosynthetic pathway that produces biotin from pimeloyl-CoA in four enzymatic steps. The final step, insertion of sulfur
Bi-Huang Hu et al.
Analytical chemistry, 79(19), 7275-7285 (2007-08-24)
We describe a new method for encoded synthesis, efficient on-resin screening, and rapid unambiguous sequencing of combinatorial peptide libraries. An improved binary tag system for encoding peptide libraries during synthesis was designed to facilitate unequivocal assignment of isobaric residues by
Rocio Rodriguez-Melendez et al.
The Journal of nutrition, 133(5), 1259-1264 (2003-05-06)
In mammals, biotin serves as a coenzyme for carboxylases such as propionyl-CoA carboxylase. The expression of genes encoding interleukin-2 (IL-2) and IL-2 receptor (IL-2R)gamma also depends on biotin. Biotin metabolites are structurally similar to biotin, and their concentrations in tissues
M Sárdy et al.
Clinical chemistry, 45(12), 2142-2149 (1999-12-10)
Tissue transglutaminase (TGc) has recently been identified as the major, if not the sole, autoantigen of gluten-sensitive enteropathy (GSE). We developed and validated an ELISA based on the human recombinant antigen and compared it to existing serological tests for GSE
Sudha Purushothaman et al.
PloS one, 3(5), e2320-e2320 (2008-05-30)
Fatty acids are indispensable constituents of mycolic acids that impart toughness & permeability barrier to the cell envelope of M. tuberculosis. Biotin is an essential co-factor for acetyl-CoA carboxylase (ACC) the enzyme involved in the synthesis of malonyl-CoA, a committed
Notre équipe de scientifiques dispose d'une expérience dans tous les secteurs de la recherche, notamment en sciences de la vie, science des matériaux, synthèse chimique, chromatographie, analyse et dans de nombreux autres domaines..
Contacter notre Service technique