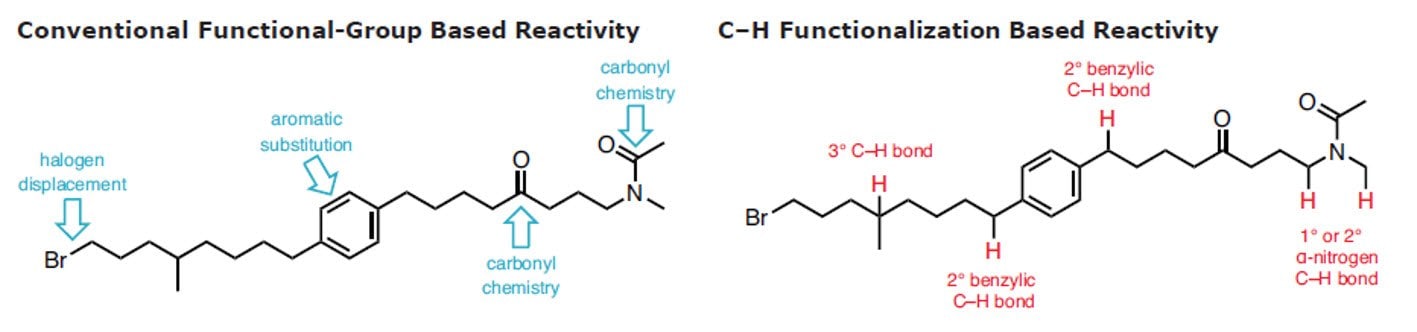
Fonctionnalisation des liaisons C–H
La fonctionnalisation des liaisons C–H est appelée le Saint Graal de la synthèse organique1. Les récents efforts déployés en chimie organique, en catalyse et dans le domaine des composés organométalliques ont débouché sur de réelles avancées en matière de compréhension de la réactivité des liaisons C–H et de développement de réactions robustes tirant parti de ces nouvelles connaissances, ce qui indique que le temps est venu d'introduire massivement ces tactiques dans le lexique de la rétrosynthèse2-11. La conversion fiable et prévisible d'une liaison C–H en liaison C–C, C–N, C–O, ou C–X de manière sélective et contrôlée permet de réduire les déchets et de limiter le nombre d'étapes de la synthèse.
De nouvelles méthodes d'activation des liaison C–H permettent d'augmenter le nombre de sites pouvant être ciblés au sein d'une molécule donnée, ce qui offre davantage de possibilités pour la transformer en produit complexe. De plus, cela permet de cibler en synthèse organique des types de liaisons chimiques complètement différents, en particulier avec une grande chimiosélectivité. Associée à la chimie traditionnelle des groupements fonctionnels, la fonctionnalisation C–H simplifie considérablement la synthèse chimique visant à construire des produits naturels et des composés pharmaceutiques complexes. Même si l'application de la logique liée à la fonctionnalisation C–H présente clairement des avantages12, de nombreux cursus en chimie organique ne reflètent pas encore cette approche. Pour en savoir plus sur ce sujet, consultez le Manuel de fonctionnalisation C–H.
Articles techniques apparentés
- Professor Karl Anker Jørgensen and his group have developed ethers which serve as excellent chiral organocatalysts in the direct asymmetric α-functionalization of aldehydes.
- The synthesis of heteroaromatic and aromatic compounds is at the heart of the chemical industry. The ever-growing demand for new chemical entities, coupled with dwindling resources and time constraints allotted to any given research project, a rapid way to diversify (hetero)aromatic scaffolds is needed.
- The Du Bois group at Stanford University has made substantial progress within the field of Rh-catalyzed C–H amination via oxidative cyclization of carbamate, sulfamate, sulfamide, urea, and guanidine substrates to give 1,2- and 1,3-heteroatom motifs masked in the form of 5- and 6-membered ring heterocycles.
- Aryl chlorides are commonly used in cross-coupling reactions and can serve as key intermediates towards the synthesis of pharmaceutical drug candidates and natural products.
- A recyclable, ligand-free ruthenium catalyst for C–H activation reactions and concomitant C–C bond formation in the presence of water.
- Afficher tout (10)
Bibliographie
Pour continuer à lire, veuillez vous connecter à votre compte ou en créer un.
Vous n'avez pas de compte ?